从第1代到“第5代”,HIV诊断技术到底有何进步?
前 言
1985年,第一个HIV抗体检测试剂问世,用于筛查血液制品。在过去30多年中,伴随着AIDS防治的需要、对HIV感染和病毒学认识的不断深入及分子生物学技术的进步,HIV血清学检测方法有了长足的进展,目前已经发展到“第5代试剂”。
第1代试剂
1983—1984年,HIV体外分离培养成功(当时称为LAV/HTLV-Ⅲ/ARV,1986年被命名为HIV),为通过病毒培养方法制备HIV抗原奠定了基础。1985年3月,美国FDA批准了第一个HIV抗体筛查试剂,用于筛查血液制品。该试剂主要根据夹心法的原理,通过间接ELISA法,检测HIV-1抗体,所用的包被抗原为体外培养的HIV裂解物,窗口期大约为3个月。
由于HIV全病毒抗原制备和纯化困难,天然的结构和表达蛋白上含有很多的交叉抗原表位,除此之外有很多杂抗原,主要HIV结构和表达蛋白浓度不能保证,导致出现很多假阴性和假阳性,灵敏度和特异性不高。尽管如此,应用第1代试剂筛查,阻断血液传播HIV的效果十分显著。
自1985年后,几乎所有的经输血传播HIV的事件都是处于窗口期的HIV感染者献血造成的,因此提高试剂的敏感性,缩短窗口期成为HIV诊断试剂发展的主要目标。
第2代试剂
20世纪80年代中后期,基因工程技术迅速发展,DNA重组和多肽合成技术出现。1990年5月,使用基因重组或合成多肽抗原的HIV诊断试剂问世。1992年2月,FDA批准了第一个HIV-1/HIV-2抗体酶免疫试剂,利用间接酶联免疫法原理,比第1代诊断试剂的窗口期缩短了20天,灵敏度和特异性也有所升高,且在包被的HIV-1抗原中加入HIV-2 gp36,也减少了第1代试剂对HIV-2抗体的漏检。
第3代试剂
为进一步提高试剂的敏感性,1994年开发出了第3代HIV抗体初筛试剂,由第1代和第2代试剂的间接法变为双抗原夹心法,酶标记物也由抗人IgG抗体改为特异性HIV抗原。第3代试剂窗口期为3周,比第2代试剂检出HIV抗体时间提前4~9天,并随后加入了gp41多肽解决了HIV-1 O群标本的诊断问题。
第4代试剂
第4代试剂可以同时检测HIV-1/2 O抗体和p24抗原,称为HIV抗原/抗体试剂,由于可以同时检测HIV抗原和抗体,是较为完善的HIV感染的筛查试剂。第4代HIV检测试剂相对于第3代HIV检测试剂来说,其检测窗口期平均提前了4~7天。
第5代试剂
第4代试剂虽然能同时检测HIV抗体及抗原,但无法区分抗体和抗原。“第5代试剂”在第4代检测试剂的基础上,双孔同时检测HIV抗体和HIV p24抗原,提高了检测灵敏度;检测结果能够区分HIV抗体和p24抗原,更有利于判断HIV感染的阶段,助力精准临床诊疗。“第5代试剂”的叫法,目前还有争议。有人认为所谓“第5代试剂”,严格讲应该也算第4代试剂。这种观点不无道理。
以下为每一代试剂的特点总结(表1)。
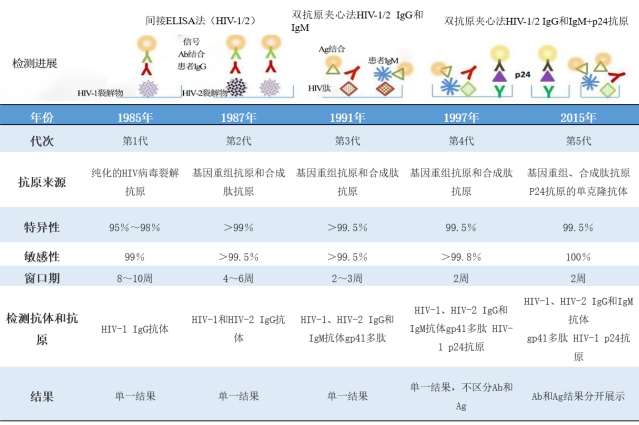 表1 HIV诊断试剂30多年的发展历程
表1 HIV诊断试剂30多年的发展历程
临床上,进行HIV感染检测时,首先进行HIV抗体的免疫检测,重复有反应的标本再用蛋白印迹试验或间接免疫荧光进行确证试验,如果为阳性则诊断为HIV-1抗体阳性。这是国际上诊断艾滋病的金标准。
《全国艾滋病检测技术规范(2020年修订版)》中新增区分抗体抗原检测试剂筛查检测流程(图1),使用区分抗体抗原检测试剂得到“抗体无反应而抗原有反应”的结果时,复检后可直接进行HIV-1核酸试验或随访,这一流程减少了检测次数,从而缩短了总检测周期,有助于HIV感染早期急性患者更快确诊。
 图1 区分抗体抗原检测试剂筛查检测流程
图1 区分抗体抗原检测试剂筛查检测流程
在20世纪90年代初HIV快速检测开始被使用,这类试验可使用血液、尿液、口腔黏膜渗出液等类型样本,包括检测抗体、同时检测抗体和抗原,操作简便快速,适用于应急检测、门诊和急诊检测、自愿咨询检测(voluntary counseling testing,VCT)及检测点等。其优势在于初级卫生保健中心的非实验室工作人员也可以为居住在偏远地区的患者提供诊断服务。
早期HIV快速检测的假阳性和假阴性结果发生率都相当高。随后,不同的检测平台,如侧流装置(测定HIV-1/2、Uni-Gold、StatPak和Ora-Quick Advance HIV-1/2)、流式细胞仪(INSTI HIV-1/2)和改良的凝集测定,极大地简化和改进了检测程序,提高了检测敏感性和特异性。这些检测平台能在30min内完成检测,INSTI HIV-1/2检测只需1min,其准确性也比较高,因此非常适合在基层和流动诊所进行检测和咨询,非实验室工作人员也可以通过标准的培训进行最快速的检测。
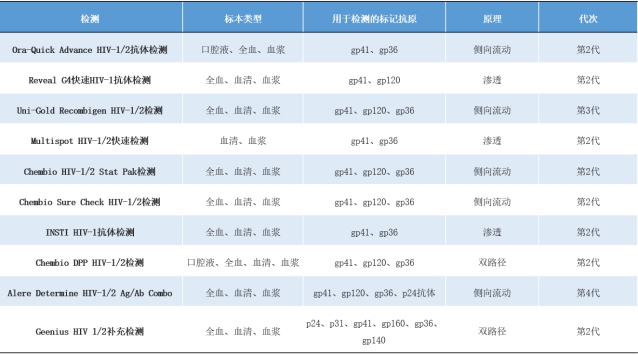
Ora-Quick Advance HIV-1/2快速检测等检测方法使用口腔液替代手指穿刺全血的样本类型,允许个人收集自己的样本进行HIV测试。美国FDA批准了VIH和INSTI的全血HIV-1/2抗体测试和Ora-Quick Advance的口腔液HIV-1/2抗体测试(表2)。
表2 经FDA批准的快速和即时HIV检测试剂
 小 结
小 结
在过去的30多年里,HIV诊断学技术不断发展,窗口期不断缩短,并且开发了多个亚型的检测,解决HIV遗传多样性的问题,不断改进的检测方法,避免误诊、漏诊,提高了检测率。HIV快速检测诊断,能及时在ART中确定HIV状态和病毒治疗效果,但也应警惕早期开展ART和使用PrEP给免疫测定的结果带来的影响。因为缺乏抗原刺激影响HIV生物标志物的产生,如果能进一步实现快速简便地进行HIV-1 RNA检测,扩大检测覆盖面,将有助于促进HIV急性感染的发现。


